Hiszpańscy naukowcy opracowali nowatorski sposób leczenia nowotworów pęcherza moczowego. Wykorzystali do tego zasilane mocznikiem nanoroboty, które precyzyjnie celują w nowotwór, atakując go radioizotopem znajdującym się na ich powierzchni. Podczas testów na myszach taka forma terapii zmniejszyła guz o 90 proc.
Nowotwór pęcherza moczowego ma jeden z najwyższych wskaźników zachorowalności na świecie. Jest czwartym pod względem częstości występowania nowotworem u mężczyzn. Ryzyko zachorowania rośnie wraz z wiekiem. Nowotwór ten charakteryzuje się częstymi nawrotami, co wymaga ciągłej obserwacji pacjenta. Dlatego też ten rodzaj nowotworu należy do najdroższych w leczeniu ze względu na powtarzające się pobyty w szpitalu i konieczność stosowania dodatkowych terapii.
Nanoroboty do walki z nowotworami stworzyli naukowcy z Katalońskiego Instytutu Inżynierii (IBEC) oraz CIC biomaGUNE we współpracy z Instytutem Badań nad Biomedycyną (IRB Barcelona) i Uniwersytetem Autonomicznym w Barcelonie (UAB). Uczeni twierdzą, że ich badania mogą utorować drogę do opracowania nowych, znacznie szybszych metod leczenia nowotworów pęcherza moczowego.
Obecne metody leczenia polegają na bezpośrednim podaniu leku do pęcherza moczowego. Jednak ich skuteczność terapeutyczna, jak wskazali autorzy nowych badań, pozostaje niska. „Te metody powodują niepożądane skutki uboczne i mają ograniczoną skuteczność, o czym świadczy odsetek nawrotów w ciągu 5 lat wynoszący 30–70 proc. i odsetek progresji wynoszący 10–30 proc.” – napisali autorzy. Nowa metoda pozwalałaby na skrócenie czasu hospitalizacji, co oznacza niższe koszty i większy komfort dla pacjentów.
Rezultaty oraz opis badań ukazał się na łamach pisma „Nature Nanotechnology” (DOI: 10.1038/s41565-023-01577-y).
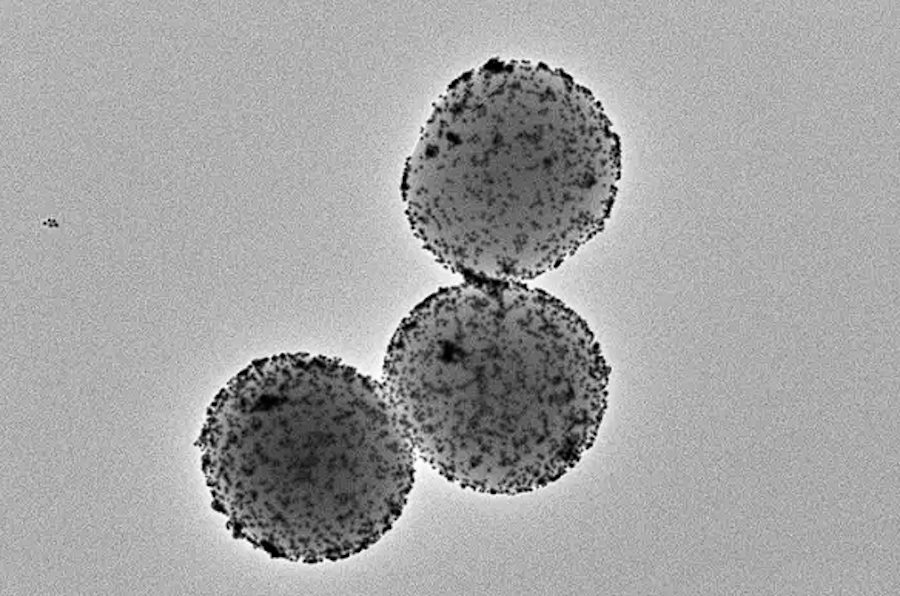
Opracowane przez hiszpańskich badaczy nanomaszyny to właściwie wykonane z krzemionki maleńkie kuleczki o porowatej powierzchni, na której znajdują się różne elementy o określonych funkcjach. Badacze umieścili tam ureazę – enzym, który reaguje z mocznikiem, dając nanorobotom napęd i umożliwiając przemieszczanie się wewnątrz organizmu. Drugim kluczowym elementem na powierzchni nanomaszyn jest radioaktywny jod - radioizotop powszechnie stosowany w miejscowym leczeniu nowotworów.
Te nanomaszyny są niezwykle obiecującą alternatywą dla obecnych metod leczenia. Naukowcy wcześniej wykazali, że zdolność nanorobotów do samodzielnego poruszania się umożliwia im dotarcie do każdej ściany pęcherza moczowego. Cecha ta jest korzystna w porównaniu z obecnie stosowanym leczeniem, gdzie po wstrzyknięciu leku bezpośrednio do pęcherza pacjent musi zmieniać pozycję co pół godziny, aby lek dotarł do wszystkich ścian pęcherza.
W nowych pracach wykazali także, że nanomaszyny są mobilne w pęcherzu i gromadzą się w pobliżu guza, a nawet do niego wnikają. Opracowali także system obrazowania wykorzystujący pozytonową tomografię emisyjną (PET) i mikroskopię fluorescencyjną. System skanuje różne warstwy pęcherza i zwraca trójwymiarowy model, umożliwiając w ten sposób obserwację całego narządu.
- Opracowany przez nas innowacyjny system optyczny umożliwił wyeliminowanie światła odbitego przez sam guz, co pozwoliło nam z niespotykaną dotąd rozdzielczością zidentyfikować i zlokalizować nanoroboty w całym narządzie bez wcześniejszego ich znakowania. Zaobserwowaliśmy, że nanoroboty nie tylko dotarły do guza, ale także do niego wniknęły, wzmacniając w ten sposób działanie radiofarmaceutyku – wyjaśnił Julien Colombelli z IRB Barcelona.
Nanomaszyny zasilane mocznikiem, substancją odpadową znajdującą się w moczu, przemieszczają się do guza i penetrują go, dostarczając radiofarmaceutyk. Już jedna dawka nanorobotów w badaniach na myszach doprowadziła do znacznego zmniejszenia się rozmiarów guza.
- Przy pojedynczej dawce zaobserwowaliśmy 90 proc. zmniejszenie objętości guza – powiedział kierownik badań Samuel Sánchez z IBEC. - Jest to znacznie skuteczniejsze, biorąc pod uwagę, że pacjenci z tego typu nowotworem mają zazwyczaj od 6 do 14 wizyt w szpitalu w ramach leczenia. Takie podejście do leczenia zwiększyłoby skuteczność, skracając czas hospitalizacji i koszty leczenia – dodał.
Ale ustalenie, dlaczego nanoroboty kierują się w stronę guza, stanowiło wyzwanie, bo nanomaszynom nie zaimplementowano specyficznych przeciwciał pozwalających rozpoznać guz. - Zaobserwowaliśmy jednak, że te nanoroboty mogą rozkładać macierz zewnątrzkomórkową nowotworu poprzez lokalne zwiększanie pH w drodze samonapędzającej się reakcji chemicznej. Zjawisko to sprzyjało większej penetracji guza i było korzystne w osiągnięciu akumulacji w guzie – wyjaśniła Meritxell Serra Casablancas z IBEC.
Precyzyjne celowanie w guza zmniejsza prawdopodobieństwo wystąpienia działań niepożądanych, a wysoka akumulacja w tkance nowotworowej sprzyja efektowi radioterapeutycznemu. - Wyniki tego badania otwierają drzwi do zastosowania innych radioizotopów o większej zdolności wywoływania efektów terapeutycznych, ale których zastosowanie jest ograniczone w przypadku podawania ogólnoustrojowego – wskazała Cristina Simó.
Źródło: IBEC, Azonano, fot. IBEC