Międzynarodowy zespół naukowców opracował nanoroboty, które zostały zaprogramowane do walki z nowotworami. Strategia maleńkich robotów polega na zmniejszeniu rozmiarów guza poprzez odcięcie do niego dopływu krwi.
Nanomedycyna w ostatnich latach zrobiła ogromne postępy. Otwiera ona drogę ku nowym terapiom z zastosowaniem najnowszych rozwiązań nanotechnologicznych. Dzięki niej możliwe jest tworzenie mikroskopijnych nanocząsteczek o rozmiarach molekuł w celu diagnozowania i leczenia trudnych chorób, zwłaszcza raka.
Ostatni sukces w tej gałęzi medycyny jest dziełem naukowców z Uniwersytetu Stanowego Arizony oraz ich kolegów z National Center for Nanoscience and Technology Chińskiej Akademii Nauk. Wyniki prac zespołu zostały opublikowane na łamach pisma „Nature Biotechnology”.
- Opracowaliśmy pierwszy w pełni autonomiczny, zrobotyzowany system DNA do bardzo precyzyjnego projektowania leków i ukierunkowanej terapii antynowotworowej – powiedział Hao Yan, specjalista od DNA origami z Uniwersytetu Stanowego Arizony. - Co więcej, ta technologia opiera się na strategii, która może być stosowana w wielu rodzajach nowotworów, ponieważ wszystkie naczynia krwionośne połączone z guzem są zasadniczo takie same – dodał.
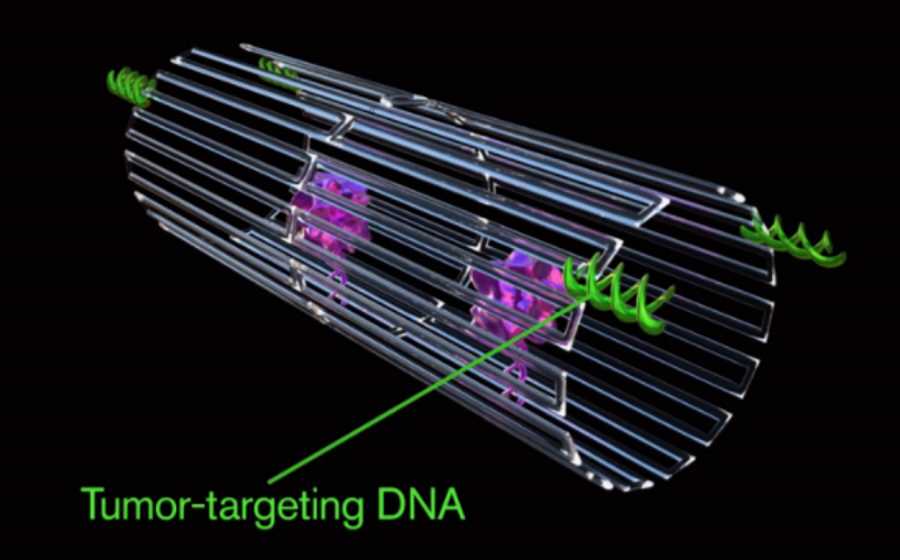
Nanoroboty wykorzystują wspomnianą już wcześniej technikę tzw. DNA origami. To metoda polegająca na tworzeniu struktur przestrzennych, które zbudowane są z nici kwasu deoksyrybonukleinowego czyli z DNA. Struktury te można modelować na różne sposoby. Mogą one przybierać różne kształty i rozmiary. Mogą być użyte także do różnych celów, chociażby do dostarczania leku w konkretne miejsce w organizmie. A wszystko to w skali tysiąc razy mniejszej niż ludzki włos.
Prace nad zrobotyzowanym nanosystemem do walki z nowotworami rozpoczęto pięć lat temu. Naukowcy najpierw chcieli odciąć zaopatrzenie guza w krew poprzez wywołanie krzepnięcia krwi przy użyciu nanonośników opartych na DNA. Następnie proces ten został zmodernizowany tak, aby był w pełni programowalnym systemem zdolnym do samodzielnego wykonywania swojej misji.
- Te nanoroboty można zaprogramować do transportu ładunków molekularnych i wywoływania blokady dostarczania krwi do guza na miejscu, co może prowadzić do śmierci tkanki nowotworowej i zmniejszenia guza – wyjaśnił profesor Baoquan Ding z Chińskiej Akademii Nauk.
Do przetestowania działania nanorobotów zespół naukowców wykorzystał dobrze znany model nowotworu myszy, w którym ludzkie komórki rakowe są wstrzykiwane myszom w celu wywołania agresywnego wzrostu guza. Gdy guz zaczął się powiększać, do akcji wkroczyły nanoroboty.
Każdy z nanorobotów ma wymiary 90 nanometrów na 60 nanometrów. Do ich powierzchni został przyczepiony enzym krzepnięcia krwi, zwany trombiną. Tak przygotowane nanoroboty zostały wstrzyknięte gryzoniom.
Jednak badacze musieli upewnić się, że trombina zostanie uwolniona w komórkach nowotworowych, a nie w zdrowych. W tym celu zaopatrzyli nanoroboty w tzw. aptamery DNA, które łączą się tylko z białkiem zwanym nukleoliną. Białko to jest wytwarzane w dużych ilościach na powierzchni komórek śródbłonka nowotworu - i nie znajduje się na powierzchni zdrowych komórek. Nanoroboty były zaprogramowane tak, by uwalniać trombinę dopiero po przyłączeniu się do tkanki guza.
W ten sposób, w ciągu kilku godzin w guzach obecnych w mysich organizmach tworzyły się zakrzepy krwi blokujące dopływ krwi do guzów prowadząc do śmierci tkanki nowotworowej.
Zespół wykazał, że nanoroboty są bezpieczne i skuteczne. Podczas testów badacze nie zaobserwowali szkodliwego wpływu pracy nanobotów na zdrowe tkanki. - Nanoroboty okazały się bezpieczne i immunologicznie obojętne - powiedział Yuliang Zhao profesor z Chińskiej Akademii Nauk.
Co najważniejsze, zespół nie znalazł dowodów na to, że nanoroboty rozprzestrzeniały się w mózgu, gdzie mogłyby powodować niepożądane skutki uboczne, takie jak udar.
Atak nanorobotów zablokował dopływ krwi do guza i spowodował uszkodzenie jego tkanki w ciągu 24 godzin, nie wywierając wpływu na zdrowe tkanki. Większość nanorobotów została usunięta z organizmu po niecałej dobie. W ciągu dwóch dni stwierdzono istnienie zaawansowanej zakrzepicy, a po 3 dniach zakrzepy obserwowano we wszystkich naczyniach nowotworowych.
System nanorobotów testowano także na myszach z czerniakiem i rakiem płuc. W przypadku czerniaka u 3 z 8 gryzoni nastąpiła regresja guzów. Jeśli chodzi o raka płuc to także zaobserwowano zmniejszenie się guzów. Średni czas życia myszy biorących udział w badaniu wydłużył się dwukrotnie – z 20,5 do 45 dni.
- Nanorobot DNA dostarczający trombiny stanowi istotny postęp w stosowaniu nanotechnologii w leczeniu raka. W mysim modelu czerniaka nanorobot nie tylko wpływał na pierwotny nowotwór, ale także zapobiegał powstawaniu przerzutów, wykazując obiecujący potencjał terapeutyczny – przyznał Yan.
- Myślę, że jesteśmy znacznie bliżsi rzeczywistym praktycznym zastosowaniom medycznym tej technologii. Kombinacje różnych nanorobotów przenoszących różne czynniki mogą pomóc w osiągnięciu ostatecznego celu badań nad rakiem. Ponadto obecną strategię można opracować jako platformę do dostarczania leków do leczenia innych chorób – podkreślił naukowiec.
Źródło: EurekAlert!, fot. Arizona State University